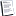
عدد تأكسد H فى NaHCO3 هو +1 حيث يكون الهيدروجين له رقم تأكسد -1 فقط فى الهيدريدات وعدا ذلك يكون +1
وإذا أردت حسابه
فأن الكربونات لها رقم تأكسد -2 دائما"
فيكون -2 + س +1 = صفر
س-1=صفر
س =+1
ولا تحتاج ذلك لأنه إذا لم يكن هيدريد (الفلز والهيدروجين فقط ولا يوجد معهم عنصر أخر ) يكون +1
-أكسيد الألومنيوم متردد لأنه يتفاعل كما قلت فى الأوساط القاعديه كأنه حمض وفى الأوساط الحامضيه كأنه قلوى
- نصف قطر الأيون السالب أكبرمن نصف قطر ذرته لأن عدد الألكترونات يكون أكبر من عدد البرتونات وبالتالى يحدث تنافر ينتج عنه تمدد مما يؤدى لزيادة نصف قطر أيون الكلور السالب عن نصق قطر ذرة الكلور
-الميل الألكترونى للفلور أكبر من الميل الألكترونى للكلور ولذلك لصغر نصف قطر ذرة الفلور مما أدى إلى تعرض الألكترون العاشر الداخل على الذرة لقوة تنافر عاليه مع التسع ألكترونات الموجودة أصلا" حول النواة فقل الميل الألكترونى للفلور عن الميل الألكترونى للكلور.
أشرح لك هذه النقطه :-
أثناء دخول الألكترون العاشر على الذرة فهو مثل أى ألكترون يدخل على أى ذرة يتعرض لقوتين قوة جذب النواةوهى التى تصنع الميل الألكترونى وقوة تنافر من الألكترونات الموجودة حول النواة وهى تنقص من الميل . وهنا فى الفلور كانت قوة التنافر عالية جدا" بسبب صغر نصف قطر ذرته فوجدت التسع ألكترونات فى حيز ضيق حول النواة فكان التنافر عالى مما قلل من الميل
-بسبب زيادة عدد البرتونات عن عدد الألكترونات فيحدث جذب لألكترونات التكافؤ عالى للداخل ينتج عنه تقلص ونقص نصف قطر الأيون الموجب للصوديوم عن نصف قطر ذرته.
أشكرك جزيلا" وأنتظر النموذج التالى
__________________
إن الله يخفى قدرته فى أسبابه
ويخفى غضبه فى معصيته
ويخفى رضاه قى طاعته
|